Квантовые числа описывают определенные свойства электрона. Узнайте об атомной орбитали, четырех квантовых числах (главное, угловой момент, магнитное и спиновое) и о том, как записывать квантовые числа на основе электронной конфигурации.
Четыре квантовых числа
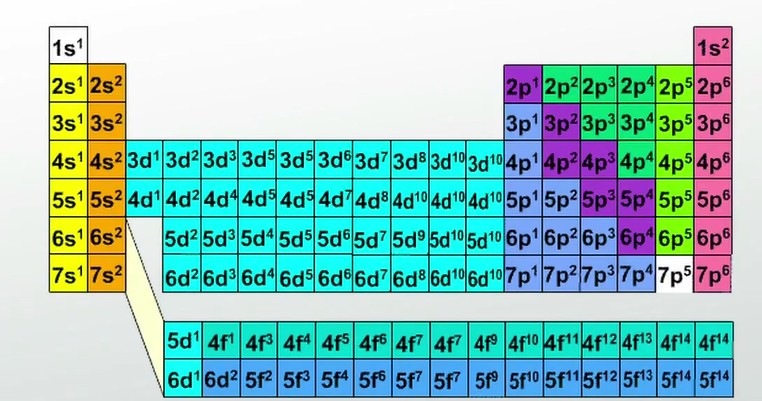
Периодическую таблицу можно использовать для определения электронных конфигураций.
Как бы вы описали кому-то, где именно вы жили? Полагаю, вы бы начали со своего адреса. Когда вы указываете местоположение здания, вы обычно указываете, в какой стране оно находится, в каком городе и штате оно находится в этой стране, а также его почтовый адрес. Как нет двух зданий с одинаковым адресом, так и два электрона не могут иметь одинаковый набор квантовых чисел . Кроме того, существуют очень специфические правила, касающиеся квантовых чисел, которые могут существовать вместе, точно так же, как нельзя сказать, что Висконсин — это штат в Испании. Квантовое число описывает определенный аспект электрона. Точно так же, как у нас есть четыре способа определения местонахождения здания (страна, штат, город и почтовый адрес), у нас есть четыре способа определения свойств электрона или четырех квантовых чисел.
Электронные конфигурации
Прежде чем приступить к этому уроку, вы должны иметь представление о том, что такое электронная конфигурация и как ее записать для элемента. Помните, что электронная конфигурация говорит нам, где находится каждый электрон в атоме, и знание расположения электронов необходимо, чтобы понять, как элемент будет реагировать и какие типы молекул он образует. Итак, начнем с атома кремния. Какова будет его электронная конфигурация? У вас должен быть ответ 1s2 2s2 2p6 3s2 3p2. Кремний имеет в общей сложности 14 электронов, и все они представлены этой электронной конфигурацией. Так что же означают все эти цифры и буквы? Этот урок поможет взломать код электронной конфигурации.
![]()
Электронная конфигурация для кремния
Прежде чем мы углубимся в подробности этих квантовых чисел, важно отметить, что, когда я говорю о местоположении, я имею в виду вероятное местоположение. На самом деле нет способа точно узнать , где находится электрон в данный момент времени; они очень неуловимы. Но можно определить, в какой конкретной трехмерной области он, вероятно, находится. Эти трехмерные границы, где наиболее вероятно находится электрон, называются атомной орбиталью.
Главное квантовое число
Первое квантовое число, описывающее электрон, называется главным квантовым числом . Его часто обозначают буквой н . Это число говорит нам об уровне энергии или размере орбитали. Чем выше число, тем больше область. Итак, давайте возьмем электронную конфигурацию кремния и посмотрим на самый последний электрон, добавленный к кремнию. Он должен быть один на 3p - орбитали. Эта цифра 3 указывает на главное квантовое число. Таким образом, для этого электрона n = 3. Орбиталь, на которой будет находиться последний электрон, будет больше, чем 2p- орбиталь , потому что она имеет более высокий номер. Это означает, что 2p - электрон с большей вероятностью будет находиться ближе к ядру, чем 3p - электрон. Вы также часто будете слышать термин «энергетический уровень», когда имеете дело с электронами и их расположением. 2 p- электрона расположены на втором энергетическом уровне, а 3 p- электроны расположены на третьем энергетическом уровне. У них будет больше энергии, чем у электронов на 2р- орбиталях . Итак, в кремнии сколько электронов будет иметь n = 3 как одно из их квантовых чисел? Ответ: 4. Есть два 3s - электрона и два 3p - электрона. Все начинают с 3, поэтому у всех будет главное квантовое число 3.
Угловой момент Квантовое число
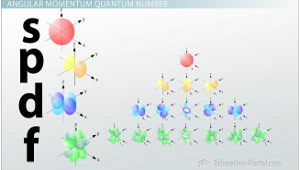
Квантовое число углового момента относится к форме орбиталей.
Следующее квантовое число относится к буквам в электронной конфигурации. Какие буквы встречались вам при записи электронных конфигураций? Вы должны были встретить s , p , d и f . Буквы обозначают квантовое число углового момента . Звучит как полный рот, но на самом деле это всего лишь форма орбитали, которую иногда обозначают буквой l . S - орбитали имеют сферическую форму, p -орбитали имеют форму гантели, d -орбитали похожи на трехмерный четырехлистный клевер, а f -орбитали имеют форму цветка. При присвоении номера каждой форме s -образные орбитали имеют l = 0, p -орбитали имеют l = 1, d -орбитали имеют l = 2, а f- орбитали имеют l = 3. Таким образом, последний электрон, который мы добавили к атому кремния на 3p- орбитали , будет иметь l = 1 и иметь форму гантели. Итак, для этого электрона n = 3 и l = 1. Вы можете заметить, что некоторые комбинации квантовых чисел будут невозможны. Например, у вас не может быть n = 1 и l = 2 для кластера квантовых чисел, потому что это означало бы, что конфигурация электронов должна быть 1 d не существует . , а 1 d электрон
Магнитное квантовое число
Следующее квантовое число указывает на положение орбиты - как она расположена в пространстве. Это называется магнитным квантовым числом и иногда символизируется ml. Независимо от того, сколько раз вы попытаетесь повернуть сферу, у вас всегда будет только одна ориентация. Это означает, что для всех s-орбиталей возможно только одно магнитное квантовое число. То есть ml = 0. p-орбитали могут иметь три разные ориентации, поэтому им присваиваются три разных магнитных квантовых числа для возможных положений орбиталей - у нас ml = -1, ml = 0 и ml = +1. Значение -1 означает, что гантели выровнены по оси x, 0 указывает, что гантели выровнены по оси z, а +1 указывает, что гантели выровнены по оси y. d-орбитали и f-орбитали немного сложнее, но знайте, что d-орбитали могут иметь 5 различных ориентаций (-2, -1, 0, +1, и +2), а а-орбитали могут иметь 7 различных ориентаций, поэтому различные положения f-орбиталей представлены как -3, -2, -1, 0, +1, +2, и +3. Тот последний электрон, который мы поместим в атом кремния, будет иметь n = 3, l = 1 и ml = либо -1, 0, либо +1, представляя три возможных положения, которые могут иметь p-орбитали.
Квантовое число спина
Конечное квантовое число имеет дело не с размером, формой или положением орбитали, а с самим фактическим электроном. Спиновое квантовое число, часто обозначаемое s или ms, связано со спином электрона и играет очень важную роль в определении магнитных свойств атома или молекулы. Каждая отдельная орбиталь может содержать до двух электронов, и каждый электрон будет иметь разный спин, представленный либо как +1/2, либо как -1/2. Таким образом, для нашего кремниевого электрона это было бы = + 1/2 или -1 / 2. На самом деле нет никакого способа определить, просто взглянув на электронную конфигурацию, какая это.